dispozitivul de baterie
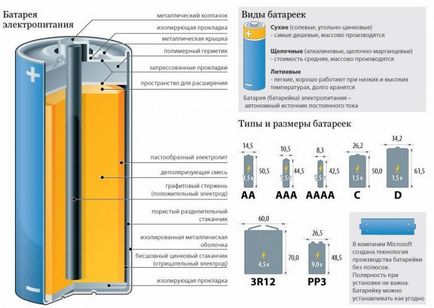
Diferite tipuri de baterii pentru o lungă perioadă de timp și au devenit parte din viața de zi cu zi. Acestea sunt utilizate în diverse dispozitive electrice cu curenti slabi, ca sursă de energie. In ciuda aparentelor diferențe semnificative, dispozitivul bateriei de orice tip are caracteristici și principii comune. Diferențele pot fi doar o parte din substanțele chimice cu care energia electrică alocată.
Bateriile unitare tipice
Bateria este fabricat în fabrică, include în structura mai multor reactivi sale chimice speciale care interacționează unele cu altele, izolate

Toți reactivii sunt separate printr-o garnitură specială care previne amestecat părțile lor componente. Cu toate acestea, această bandă poate trece electrolitului în interiorul bateriei în formă lichidă. Între diferite reactant solid și un electrolit lichid au loc reacții chimice, rezultând în formarea sarcinilor pozitive și negative. taxa Polaritatea depinde de compoziția chimică a unui reactiv. Garnitura situată între ele, nu permite să neutralizeze sarcină pozitivă și negativă.
Elemente suplimentare ale bateriilor
Pentru a elimina taxa și ieșire-l la contactele din interiorul reactiv colector curent anod este plasat într-un știft special. Catod colector curent este localizat sub manșonul exterior, care este cochilia. Ambele colectoare de curent, se termină în contactele electrice, respectiv, anod și catod. Funcționarea începe cu reacția chimică are loc atunci reactivii încărcați separarea și transferul lor ulterior la colectorii de curent. În cele din urmă, taxele furnizate electrozii izolați și direct în dispozitivul electronic.
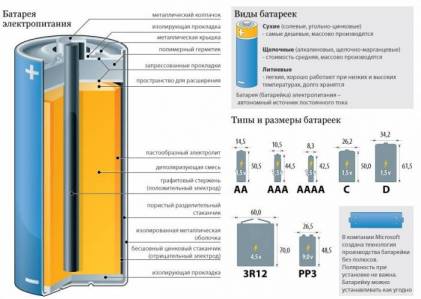
Dispozitivul de baterii alcaline (alcaline) utilizat de zinc sub formă de pulbere. Pentru a incetini consumul de zinc, au fost făcute unele aditiv în urmă timp în elemente chimice cu pulbere - mercur și cadmiu. Din moment ce aceste suplimente au fost daunatoare, care le-au încetat să se aplice. În modelele actuale bateriile sunt folosite substanțe mai scumpe, dar mai puțin nocive, cum ar fi indiu, plumb, și altele. Ca anod de reactiv utilizat în asociere cu electrolit oxid de mangan, care în acest caz este alcalin.
Bateriile alcaline pot apărea uneori. Acest lucru se întâmplă atunci când leakproof datorită posibilei deteriorări exterioare a bucșei sau când presiunea internă devine mai mare decât în mod normal.
Bateriile saline au o structură similară și un cost mai mic. diferența lor principală este aceea că masa catod se înlocuiește cu carcasă de zinc. troleu carbon este centrat. Chloride este utilizat ca electrolit, altul decât sarea acidului clorhidric. Că ea a servit ca nume pentru acest tip de baterii.