Aminele - Enciclopedia chimică
AMINES [de la ora (MIAK)], derivați de NH3. atomii de H din k-ryh substituit pe org. Reziduuri R. În funcție de numărul de R este împărțit în amine RNH2 primare. RR'NH R'R secundar și terțiar "N; R, R“, R" mb identice sau diferite. Sootv.-NH2 numit. o amină primară, și--vtorichnoy terțiară. Conform cu numărul de grupări amino din molecula distinge mono-, di-, tri-, și poliamine.
Nume amine formate din nume org. reziduurile legate de atomul de N, de ex. CH3 NH2 -metilamina, CH3 NHS3 H7 - metilpropilamină, (C2 H5) 3 N - trietilamină. De asemenea, folosit numele format prin adaugarea prefixului „amino“, „diamino“ etc. la desemnarea hidrocarbura generice. de exemplu, compușii de tip C2 H5 CH (NH2) CH2 CH3 - 3-aminopentan. Multe hidrocarburi aromatice. Aminele sunt nume triviale, de ex. C6 H5 NH2 - anilină. CH3 C6 H4 NH2 - toluidine și OS6 H4 CH3 NH2 - anisidină (respectiv de la "toluen" și din "anisol."). alifatich superior. Structura normală, uneori numite amine. numele radicalilor grași la-t, din care unul a fost sintetizat amine, de exemplu. stearilamină. trilaurilamin.
Spectrele IR Caracteristica întindere vibrațiilor legături NH în p-D observat pentru alchilamine primare în regiunile 3380-3400 cm-1 și 3320 la 3340 cm-1; pentru aromatice primare. Aminele - două benzi de absorbție în regiunea 3500-3300 cm -1 (datorită vibrațiilor simetrice și asimetrice de intindere ale legături N-H); pentru alifatich. și hidrocarburi aromatice. secundar amiov-o singură bandă, respectiv. în regiunea 3360-3310 cm-1 și 3500-3300 cm -1 regiune; amine terțiare în acest domeniu nu absorb. In spectrele RMN chimice. schimbare proton amino de 1-5 ppm Alifatich. amine în UV și regiunile vizibile nu absorb de hidrocarburi aromatice. aminele din spectrele UV au două benzi de absorbție datorate joncțiuni.
alchilaminele, baze puternice. arilamine mai puțin viespile novny. În interacțiunea. mineral-ter amine pentru a forma săruri. în majoritatea cazurilor, p-în solubil în apă. RNH2 + HK1 -> [RN3] Cl -. Atunci când reacția. de ex. amine primare cu halogenuri de alchil amine conduce la obținerea amestecurilor de diferite grade de alchilare. și săruri cuaternare de amoniu.
Atunci când încălzirea. cu carbon-ter, anhidridele lor. cloro-esteri sau anhidride, primari și amine secundare acilată pentru a forma amide N-substituite, de ex. RNH2 + CH3 COOH -> RNHCOCH3 + H2O Anhidride reacționează în condiții blânde, chiar mai ușor - cloruri. k-acilare se efectuează în prezența rymi. de bază. Legarea formată în p-TION HC1. Când policondensarea diaminelor cu poliamide dicarboxilici la-ter, esterii acestora sau cloruri acide sunt formate. Aminele acilate au comunicare-vă slab de bază.
Sub acțiunea HNO2 alifatich. aminele primare sunt transformate în alcooli cu N2 alocarea și H2O, secundare - N-nitrozamine în R2 NNO. Aminele terțiare cu obișnuitul t-re cu HNO2 nu reacționează. P-TION cu HNO2 utilizat pentru a identifica alifatich. amine. În interacțiunea. primar aromatic. sare HNO2 amină diazoniu formată într-un mediu acid. ArNH2 + HNO2 + HK1 -> ARSL - + 2H2 O. În aceleași condiții, secundare aromatice. Aminele sunt transformate în N-nitrozamine, terțiară - derivați de para-nitrozo. alitsiklich primar. alcooli formă amine HNO2. care este adesea însoțită de contracție sau expansiune ciclu (a se vedea. Demyanova rearanjare).
Alifatich. primare și aminele secundare de interacțiune. cu C12 sau Br2. formând un N-halo. Aminele primare cu fosgen pentru a forma un izocianat RNCO SOS12 sau uree disubstituiți (RNH) 2 CO, amine secundare - uree tetrasubstituită R2 NCONR2. Aminele primare interacțiune ușoară. cu aldehide. oferind azomethines (baze Schiff), de exemplu.
În reacția aminelor primare și secundare cu etilenă clorohidrinei formată derivați de hidroxietil, cum ar fi: C6 H5 NH2 + S1SN2 CH2OH -> C6 H5 NHCH2 CH2OH + HCI. In cele mai multe cazuri, sinteza acestor același comp. se utilizează oxid de etilena. Reacționează cu amine Lesko în prezența. număr mic în H2O:
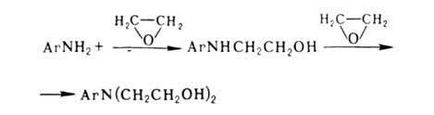
Deoarece rata de alchilare pe prima și a doua etape sunt aceleași, pentru obținerea derivatului monoalchii de oxid de etilenă este luată într-o cantitate mult mai mică de calculat.
derivați de Tsianetilnye ai aminelor primare și secundare obținute p-TION de acrilonitril în prezența. la-te sau alcaline. ArNH2 + CH2 = CHCN -> ArNHCH2 CH2CN. alifatich primar și secundar. amine în interacțiunea. formează săruri cu ditiocarbamați alchil CS2:
Atunci când încălzirea. primar aromatic. Aminele cu CS2 în prezență. alcalii formate derivați de diariltiomocheviny la-ryh acceleratori de vulcanizare -Important.
Clorhidrați de amine terțiare în timpul încălzirii. cu dil. la-ter dezalkiliruyutsya: (CH3) 3 HCl -> (CH3) 2 NH + CH3 C1.
Sub influența oxidanți puternici. de ex. KMnO4. alifatich primar. Aminele sunt convertite la amestec în, într-un roi predomină aldehide. primar aromatic. Aminele - la chinone și derivați ai acestora, alifatich secundar. și hidrocarburi aromatice. Aminele - la hidrazină tetrasubstituită. În oxidarea acțiunii aminelor terțiare H2 O2 sau peracizi generate N-oxizi de amine.
Prin substituirea nucleului în seria aromatică. amino amină electrofil orientează. orto și para-poziții, și în mediile foarte acide, datorită atom protonare N - și în poziția meta. Nitrarea primar aromatic. Aminele complicate prin oxidarea lor. cu toate acestea amină pre-acilat.
DOS. Ind. metode de sinteză. aminice
1. interacțiune. alcooli cu NH3 (amonoliză alcooli) în prezența. catalizatori de deshidratare (de exemplu. A12 O3. SiO2. ThO2. aluminosilicați. fosfați metalici) la 300-500 ° C și 1-20 MPa. Acest lucru produce un amestec de amine primare, secundare și terțiare. ROH + NH3 -> RNH2 R2 NH RAN-ul; Aminele disproporționare simultane. 2RNH2 -> R2 NH + + NH3. R2 NH + RNH2 -> R3 N + NH3. 2R2 NH -> R3 N + RNH2. Această metodă este folosită pentru insule de producție alifatich mai mici. amine. și în special metil și etilaminele. Sinteza însoțită de formarea mijloace. Numărul în subproduse - olefine.
Dacă NH3 în loc să folosească amine primare sau secundare, se obțin și amine terțiare secundare (sau). Această metodă (aminoliză) a circulat pentru insule de producție N-alchil și N, N-dialkylanilines. Ea a dezvoltat o metodă similară pentru producerea de interacțiune anilină. fenol cu NH3. Este ușor să reacționeze cu Naftoli NH3. naftilamine formează (vezi. reacția Bucherer).
2. Restaurare. aminare alifatich. și tsikloalifatich. în prezența alcoolilor. H2 pe catalizatorii de hidrogenare-dehidrogenare (N1, Co, Cu-a promovat Fe). Procedeul se realizează la 150-250 ° C și 0,1-5 MPa:
Alcoolii pot fi utilizate în loc de aldehide sau cetone; formând astfel un amestec de amine primare și secundare.
3. Katalitich. hidrogenarea nitrililor (kat.-Ni sau Co) la 100-130 ° C și 0,1-10 MPa. Cu randamente bune amine primare în amestec secundar:
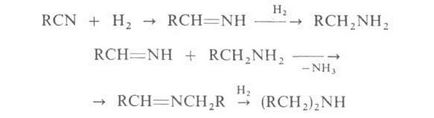
Această metodă este folosită cap. arr. pentru insule de producție de primar superior și alifatich secundar. structura normală a aminelor.
5. amide alifatich P-TION. și hidrocarburi aromatice. un carboxilic-t-p ramia alcaline C12. I2 sau Br2 pentru a forma amine primare. În acest caz, catena de carbon este redus cu un atom (reacția Hofmann).
6. P-TION cu halogenuri de alchil și arii. Prin condensarea ftalimidei cu halogenuri de alchil la ultima. hidroliza (a se vedea. Gabriel de reacție) sunt aminele alifatice primare pure.
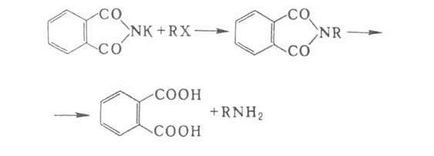
halogenuri de arii reacționează cu NH3 și amine dificile, astfel încât în bal-IFPS folosi Conn. la un ryh puternic substituenți atrăgători de electroni activat halogen, mai frecvent nitro sau sulfo. În acest fel, decembrie difenilamină și derivați de nitroaniline.
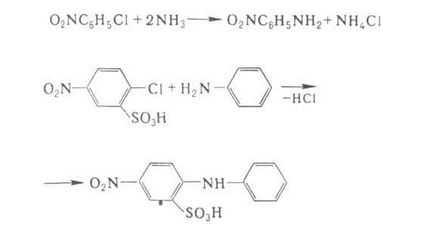
Amonoliză și aminoliza halogenuri de arii cu halogen neactivată necesită utilizarea Ser. Cu drept catalizator.
7. nitrosation N, N-dialkylanilines o placenta. hidroliza (preparare alifatich amină secundară pură.):
In laborator sintetizate aminele, de ex. p-tiile Wallach, Delepine, Curtius, Leuckart, pierdere, Mannich.
Specificitatea. p-TION detectare amine. aminele primare cu încălzire. cu CHC13 în prezență. alcaline transformate in izonitrilii. având un miros foarte picant: RNH2 + CHC13 -> RNC + ZNS1; amine secundare în procesarea HNO2. postnatal. fuziune precipitatul obținut cu fenol și acidularea cu HCI conc. H2 SO4 apare culoarea verde. Pentru a identifica primare și aminele secundare sunt utilizate în acilarea amide. Pentru cantitățile. determinarea aminele folosite metode Kjeldahl și Van Slyke (pentru alifatich primară. Aminele) bromometrich. metoda de titrare p-to-stabilite în medii apoase și neapoase, cromatografia gaz-lichid. Primar aromatic. amine, de asemenea, determinată fotometric după formarea bazelor Schiff corespunzătoare sau compuși azo.
Alifatich. Aminele afectează sistemul nervos care provoacă tulburări de permeabilitate a pereților vaselor de sânge și a membranelor celulare. f-tiile distrofie hepatică și dezvoltare. Aromatice. amine determina formarea de methemoglobină. centru de inhibare. sistemul nervos. Nek- aromatic. Un carcinogeni, cauzand cancer de vezică urinară la om (de ex. P-naftilamina, benzidină. 4-aminobifenil).
===
App. Literatura pentru articol, „Amin.“ Ternov Modern Organic Chemistry. per. din limba engleză. T 2, Moscova, 1981.; chimia organică totală. per. din limba engleză. vol. 3, M. 1982, p. 11-91, 168-228; Ulmanns Encyklopadie, 4 Aufl. Bd 7, Weinheim 1974: Kirk-Othmer enciclopedie, 3 ed. v. 2, N.Y. .- [a.o.], 1978, p. 272-376. BV Salol.