aminele alifatice
Aminele - derivați de amoniac în care atomii de hidrogen sunt înlocuiți cu radicali de hidrocarburi. Aminele sunt clasificate în funcție de numărul de atomi de hidrogen substituiți la radicalii hidrocarbonați. Distinge pervichnyeR-NH2. vtorichnyeR2-NH-N tretichnyeR3 și amine.
Sunt compuși cunoscuți cu un atom de azot cuaternar - sare de amoniu - R4N + X. În acest caz, azotul poartă o sarcină pozitivă.
În funcție de tipul de amine alifatice și aromatice radical se disting:
amine grase (aminelor grase)
Izomerie între aminele alifatice legate radical de hidrocarbură și substituenții izomerism pe atomul de azot.
Multe amine au nume triviale. Pentru raționale aminele denumirea din nomenclatura formate din resturi de hidrocarburi nume asociate cu atomul de azot și -aminei închidere:
izopropilamină, metiletilamină izobutilamină
În conformitate cu nomenclatura IUPAC pentru amine simple folosind numele rațional. În conformitate cu regulile IUPAC la numele adăugat la sfârșitul aminei radical hidrocarbonat. Lanțul de hidrocarbură începe cu atomul de carbon legat la gruparea amino: CH3CH2CH2CH-NH-CH3 1-metilbutilamină. În prezența altor grupări funcționale pe gruparea amino notată cu prefixul: NH2-CH2CH2-OH - 2-aminoetanol.
Metodele de preparare a aminelor alifatice
1. haloalcani amonoliză.
După încălzirea haloalcani cu o soluție alcoolică de amoniac într-un tub etanș, un amestec de compuși. În reacția amoniacului cu alchilamine primare halogenclorură formare. Monoalchilamine sunt nucleofile puternice decât amoniacul; ele reacționează în continuare cu un haloalcan pentru a da cantități semnificative de amine secundare și terțiare, și sare de amoniu, chiar cuaternară:

Amonoliză halogenate se referă la reacții de substituție nucleofilă. În particular, reacția are loc CH3CH2Cl + NH3 conform mecanismului:
Prin urmare, aminele primare sunt obținute în general în alte moduri.
2. alcooli amonoliză.
Se compune din înlocuirea atomilor de hidrogen în amoniac sau amină în gruparea alchil. Aceasta este o metodă importantă pentru sinteza aminelor:
Alcoolii amonoliză aplicate pe scară largă pentru sinteza aminelor alifatice inferioare (metil și etil). Acestea sunt utilizate drept combustibil pentru motoarele rachetă cu combustibil lichid și ca intermediari de sinteză organică (prepararea altor amine dimetiihidrazină anionooobmennyh rășini și substanțe anionice, pesticide, carbamați și ditiocarbamați).
3. Gabriel Synthesis.
Gabriel Sinteza aminelor primare permite pentru a obține gratuit de la un produs vysokoalkilirovannyh. Alchilarea ftalimidă mecanism SN2 de potasiu dă N -alkilftalimid care pot fi ușor hidrolizat la amina corespunzătoare:
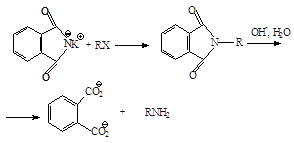
Ftalimida este preparată prin încălzirea anhidridă ftalică cu amoniac:
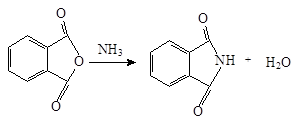
Ftalimidă posedă proprietăți acide datorită delocalizării sarcinii negative asupra acil doi atomi de oxigen pentru anioni imidă. Acesta pierde un proton legat de azot, prin reacția cu o bază de potasiu tip hidroxid. ftalimidă ion format în această reacție - anion care stabilizează:
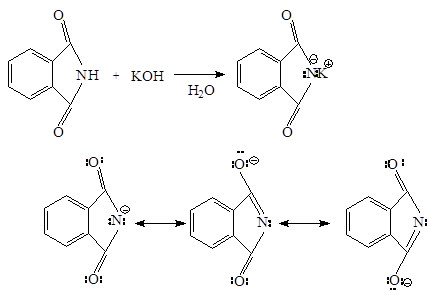
4. Aminarea reductivă a compușilor carbonilici
Mulți compuși carbonilici sunt transformați în aminele în timpul procesului de recuperare, în prezența amoniacului. Recuperarea este efectuată fie prin hidrogenare catalitică sau folosind cianoborohidrură de sodiu NaBH3CN. Mecanismul acestei reacții implică două etape principale: formarea iminei și iminei la recuperarea aminei:
Dacă în loc de amoniac utilizată o amină primară, produsul de reacție este o amină secundară.
5. Restaurarea nitroalcani, oxime, nitrili, amide
Conține azot compus (nitroalcani, oxime, amide, nitrili și izonitrilii) sub hidrogen sau un alt randament de reducere sau amine primare sau secundare sau un amestec al acestora:
Catalizatori - Pt, Pd, Ni.
3. Scindarea amide acide (rearanjarea Hofmann).
Amidele acizilor carboxilici alifatici și aromatici reacționează cu soluții alcaline de iod, brom sau clor pentru a forma amine primare. Această așa-numită hypohalogenite reacție Hofmann nu poate sintetiza numai amine primare, dar, de asemenea, scurta lanțul pe atomul de carbon.
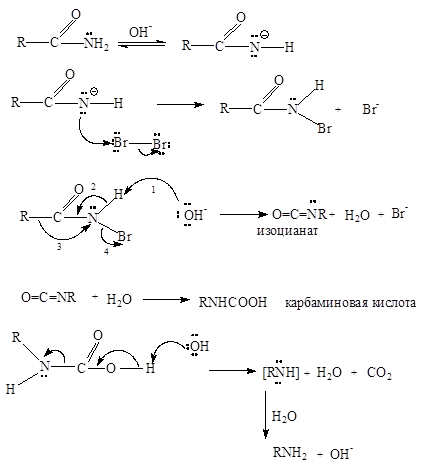
Mai întâi de rezonanță stabilizată ion de amidă formată amidă N-halogenat (de aici amidele bromo N-), care este instabil în soluție alcalină și convertită în izocianat.
Izocianații, precum și analogii lor de carbon (ketenes) reacționează rapid cu apa. hidratare karbaminovayakislota produs. ușor decarboxilat pentru a forma amina.
7. rearanjarea Curtius.
cloruri acide, interacționând cu NaN3 azidă de sodiu. da azide (azide acide) care, atunci când sunt încălzite, sunt transformate în izocianați:
Conversia azide acil în izocianații, așa cum se arată mai jos, este un proces coordonat. Această reacție se numește Rearanjarea Curtius:
Apoi, izocianații reacționează cu aminele de apă și forma:
aminele primare și secundare capabile să formeze legături de hidrogen intermoleculare. Prin urmare, aminele au puncte de fierbere mai ridicate decât compușii nepolari cu aceeași greutate moleculară. Alcooli și acizii carboxilici formează legături de hidrogen mai puternice decât aminele. Deoarece aminele terțiare nu conțin atomi de hidrogen de la atomul de azot, ele nu formează legături de hidrogen.
aminele cu greutate moleculară mică sunt amestecate cu apă în orice proporții.
aminelor. amine aromatice
Proprietățile chimice ale aminelor
1. Reacția aminelor cu acizi
Aceste săruri prin reacție cu soluții apoase de baze a fost amine izolate.
Bazicitatea aminelor este determinată de ușurința cu care clivează protonul amina din apă.
2. Alchilarea aminelor cu halogenclorură - vezi Lecture №31 .. În ultima etapă se formează sare cuaternară de amoniu - cele patru grupe organice sunt legați covalent la atomul de azot, sarcina pozitivă este echilibrată de prezența ionilor negativi:
baze cuaternare de amoniu (substanță albă cristalină) de bazicitate comparabile cu NaOH, KOH.
4. Acilarea aminei (prepararea amidelor).
Aminele primare și secundare reacționează cu anhidride și halogenuri acide, pentru a forma amide:
amide substituite denumite ca derivați ai amidelor nesubstituiți ai acizilor carboxilici.
Formată în cantitatea echivalentă de reacție de acid se leagă amină nereacționat. O astfel de metodă devine neeconomic dacă amina dificil de sintetizat sau este un reactiv scump. De aceea, adesea acilată amine prin reacția Schotten-Baumann. care cuprinde reacția aminei și agentul de acilare, în prezență de hidroxid de sodiu apos:
Aminele aromatice pot fi pervichnymiArNH2 (anilină, toluidine) vtorichnymiAr2NH (difenilamină) și tretichnymiAr3N (triphenylamine).
Metodele pentru prepararea aminelor aromatice
1. Restaurarea compușilor nitro (reacția Zinin).
Ca agenți reducători utilizate fier și acid clorhidric sau acid sulfuric, staniu și acid clorhidric, hidrogen sulfurat și sulfuri alcaline, hidrosulfiți, hidrogen, în prezența catalizatorilor. Recuperarea poate fi, de asemenea, efectuată pe cale electrolitică.
În funcție de natura recuperării mediului este de moduri diferite. Într-un mediu acid ca intermediari formați și derivați nitrozo hidroxilamină. Acestea din urmă pot fi obținute ca produse finale reducerea într-un mediu neutru. Într-un mediu alcalin, procesul este mai complicat. Ca urmare a compușilor nitrozo azoxy derivați, compuși azo și apoi, în final, gidrazosoedineniya și amine.
2. arii halogenuri de amonoliză (halogenuri de arii de alchilare amoniac).
Aminele aromatice sunt preparate din halogenuri de arii și amoniac:
Datorită mobilitate redusă a unui halogen, reacția trebuie efectuată la presiuni si temperaturi ridicate în prezența catalizatorilor - cupru și sărurile sale. Numai în acele cazuri în care a - sau p este halogen la poziția p puternic grupă electronegativă, de exemplu, nitro, halogen ușor înlocuită cu o grupare amino.
3. Reacția Hoffmann.
Aminele aromatice pot fi de asemenea obținute din acizi prin amidă prin reacția Hofmann (vezi. Lektsiyu№31).
4. Prepararea aminelor aromatice secundare.
amine secundare aromatice sunt preparate prin încălzirea sărurilor de amine aromatice ale acestora:
Aminele alifatice aromatice secundare sunt preparate prin alchilarea aminelor aromatice primare, alcooli sau derivați halogenați.
5. Aminele terțiare.
Aminele aromatice terțiare sunt preparate prin alchilarea sau arilarea unei amine primare sau secundare:
Mai puțin disponibile amine aromatice terțiare preparate prin încălzirea amine secundare cu arii iodurile în prezența pulberii de cupru:
Proprietățile chimice ale aminelor aromatice
Aminele aromatice au caracter bazic mai puțin pronunțat decât alifatic. Astfel metilamină kb este 4,4 × 10 -5. întrucât anilină kb = 3,8 x 10 -10. Reducerea bazicitatea anilinei comparativ cu aminele alifatice explicate prin reacția azotului singură pereche de electroni din ciclul aromatic cu electroni - conjugarea lor. Conjugarea reduce capacitatea perechii de electroni unshared de atașarea unui proton.
Prezența grupărilor electroatrăgătoare la baza reducerii principalului. De exemplu, constanta de bazicitate aproximativ -, m - și p -nitroanilinov este în mod adecvat 1 × 10 -14. 4 × 10 -12 și 1 x 10 -12. Efectuarea unui al doilea nucleu aromatic, de asemenea, reduce semnificativ bazicitatea (la Difenilamină Kb = 10 -14 x 7,6). Formele difenilamină extrem de soluții hidrolizabile de sare numai cu acizi tari. Proprietățile de bază Triphenylamine, practic, nu posedă.
Pe de altă parte, introducerea de grupări alchil (grupări donoare de electroni) crește bazicitate (Kb N-metilanilină și N, N-dimetilanilină sunt respectiv egale cu 7,1 x 10 -10 și 10 -9 1,1 ×
1. Alchilarea aminelor aromatice.
Aminele aromatice pot înlocui hidrogenul de pe amino alchili. Această reacție conduce la amine secundare și terțiare:
Alchilarea sunt alcooli sau chloroalkane utilizați drept catalizatori de sare cuproasa ca complecși de amoniu. Este important ca procesul de N- alchilare este serie-paralel, datorită faptului că amina rezultată, la rândul său poate reacționa cu un agent de alchilare. Compoziția produselor depinde de raportul dintre reactivi.
2. Acilarea aminelor aromatice.
Acțiunea agenților de acilare (acizi, anhidride, cloruri acide), atomii de hidrogen sunt înlocuiți cu radicali amino acil.
Acil derivații nu au proprietăți de bază. Ele sunt rezistente la agenți de oxidare și de aceea sunt utilizați ca intermediari în reacțiile aminelor în prezența de oxidanți (de exemplu, nitrare).
3. Sinteza azomethines (baze Schiff).
Cu încălzire aromatice amine primare blânde cu aldehide aromatice sunt formate ușor așa numitele azomethines sau bază Schiff:
Sub acțiunea bazei Schiff acid diluat hidrolizat la aldehida și amina.
4. Reacția aminelor cu acid azotos.
HONO acid azotos instabil, dar soluția sa apoasă poate fi preparată prin dizolvarea nitrit de sodiu sub răcire în acid diluat, de exemplu, acid clorhidric.
Aminele alifatice primare reacționează cu acid azotos apos rece, pentru a forma săruri alkildiazonievyh. care se formează prin descompunerea unui amestec de produse diferite:
Aminele alifatice secundare reacționează cu acid azotos pentru a forma N-nitrozamine galben. Acești compuși, amide ale acizilor nitrici sunt baze foarte slabe.
N -nitrozodimetilamin (cancerigenă!)
complex format prin reacția unui amestec de alchilamine terțiare cu acid azotos.
Cei mai importanți reprezentanți ai aminelor aromatice
Anilina a fost mai întâi obținut prin distilarea indigo cu var (1826). În 1842 a primit reducerea Zinin de nitrobenzen. Cantitățile mici găsite în gudronul de huilă. Preparat din nitrobenzen industrial prin hidrogenare catalitică cu catalizator de cupru în fază gazoasă. Anilina în cantități mari vine vorba de culori, ciclohexilamina, caprolactamă, pesticide și altele.
p-toluidină este utilizat pe scară largă în fabricarea de coloranți, în special magenta.
N, N-dimetilanilina este utilizat la fabricarea coloranților și explozivi.